USA
FDA aprova cloroquina e hidroxicloroquina para tratamento emergencial de coronavírus
01/04/2020 às 09:43
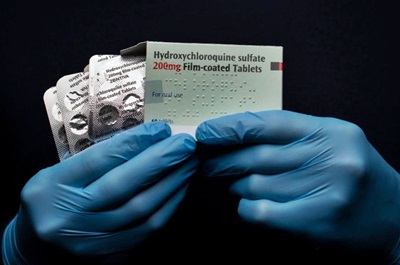 O FDA, a Administração de Alimentos e Medicamentos dos EUA, emitiu uma autorização de emergência para tratamentos experimentais de coronavírus usando os medicamentos anti-malária cloroquina e hidroxicloroquina, apesar de provas clínicas inconclusivas de sua eficácia.
O FDA, a Administração de Alimentos e Medicamentos dos EUA, emitiu uma autorização de emergência para tratamentos experimentais de coronavírus usando os medicamentos anti-malária cloroquina e hidroxicloroquina, apesar de provas clínicas inconclusivas de sua eficácia.
O Departamento de Saúde e Serviços Humanos (HHS, na sigla em inglês) disse, no domingo (29), que os produtos podem “ser distribuídos e prescritos pelos médicos para pacientes adolescentes e adultos hospitalizados com Covid-19, conforme apropriado, quando um ensaio clínico não estiver disponível ou viável”.
A entidade disse que a alemã Sandoz já forneceu 30 milhões de doses de hidroxicloroquina ao suprimento médico do governo federal para emergências de saúde pública, enquanto a Bayer doou 1 milhão de doses de cloroquina.
A agência está acelerando um processo que geralmente leva anos, enquanto o FDA conduz ensaios clínicos em Nova York, um dos epicentros norte-americanos do vírus.
O HHS disse que a autorização de emergência foi emitida porque os benefícios potenciais do produto superam os riscos e reconheceu que relatórios anedóticos sugerem que esses medicamentos podem oferecer algum benefício no tratamento de pacientes com Covid-19 hospitalizados, mas” ensaios clínicos são necessários para fornecer informações científicas. evidência de que esses tratamentos são eficazes”.

Comentários


 O FDA, a Administração de Alimentos e Medicamentos dos EUA, emitiu uma autorização de emergência para tratamentos experimentais de coronavírus usando os medicamentos anti-malária cloroquina e hidroxicloroquina, apesar de provas clínicas inconclusivas de sua eficácia.
O FDA, a Administração de Alimentos e Medicamentos dos EUA, emitiu uma autorização de emergência para tratamentos experimentais de coronavírus usando os medicamentos anti-malária cloroquina e hidroxicloroquina, apesar de provas clínicas inconclusivas de sua eficácia.



























